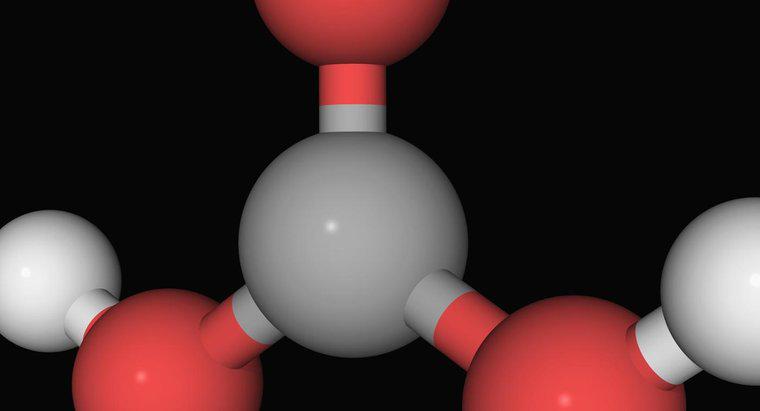
Amoniac, một hợp chất khí của một nguyên tử nitơ liên kết với ba nguyên tử hydro, không phải là bazơ mạnh. Nó là một bazơ yếu hơn thường phải phản ứng với nước trước khi phản ứng với axit. Trước khi trung hòa axit trong dung dịch, nó phản ứng với nước để tạo thành các ion amoni và hydroxit. Amoni là một ion dương của một nguyên tử nitơ và bốn nguyên tử hydro, và nó là một axit yếu.
Tất cả các bazơ hoạt động bằng cách nhận các ion hydro, chỉ là các proton trần. Điều này trung hòa axit, vì axit hoạt động bằng cách giải phóng các ion hydro để phản ứng với các vật liệu khác. Bazơ phản ứng với các ion này mạnh hơn các vật liệu khác, và do đó chúng có thể bảo vệ các vật liệu khác này khỏi axit. Tuy nhiên, bản thân các đế có thể bị ăn mòn.
Bazơ mạnh nhất, chẳng hạn như natri hydroxit, hoạt động bằng cách phân ly các ion hydroxit của chúng trong dung dịch. Các ion hydroxit phản ứng rất mạnh với các ion hydro để tạo thành nước. Các thành phần khác của axit và bazơ thường liên kết với nhau dưới dạng muối. Tuy nhiên, amoniac không chứa các ion hydroxit. Đầu tiên nó phải phản ứng với nước để tạo ra chúng. Điều này không chỉ thêm một bước trước khi trung hòa axit, mà nó còn bị phản tác dụng một phần bằng cách tạo ra amoni, một axit yếu hơn.