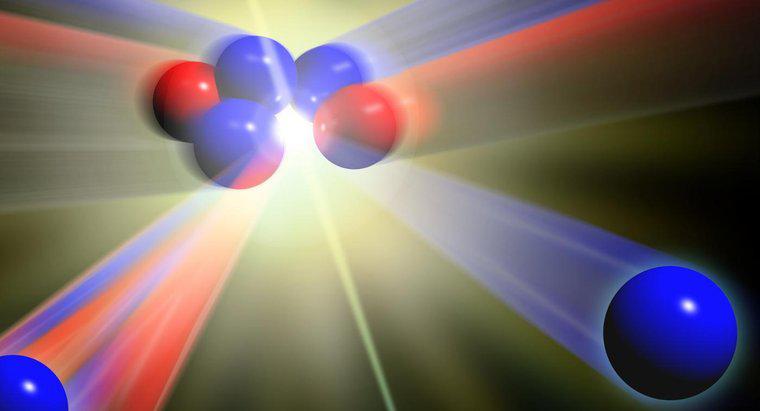
Sự khác biệt giữa nguyên tử, ion và đồng vị là số lượng hạt hạ nguyên tử. Nguyên tử là khối cấu tạo cơ bản của vật chất, là phân tử nhỏ nhất của một nguyên tố tồn tại và không thể phân chia về mặt hóa học. phương tiện thông thường. Mỗi nguyên tử bao gồm proton, neutron và electron. Trong các ion, số lượng electron khác nhau, và trong các đồng vị, số lượng neutron khác nhau.
Theo Visionlearning.com, một nguyên tử điển hình không có điện tích vì số proton mang điện tích dương bằng số electron mang điện tích âm. Tuy nhiên, số lượng điện tử trong nguyên tử có thể thay đổi bằng cách nhận thêm điện tử từ các nguyên tử khác hoặc bằng cách nhường một hoặc nhiều điện tử của nó cho các nguyên tử lân cận. Khi số electron của nguyên tử thay đổi, nguyên tử đó mang điện tích. Nguyên tử mang điện này được gọi là ion.
Thông thường, một nguyên tử có cùng số proton và neutron. Một số nguyên tử đạt được hoặc mất đi một neutron. Khi số lượng nơtron trong nguyên tử thay đổi, một đồng vị được hình thành. Các đồng vị của một nguyên tử có khối lượng nguyên tử khác nhau và thể hiện các tính chất khác nhau, nhưng chúng vẫn là cùng một nguyên tố.
Nguyên tử của một nguyên tố luôn có cùng số proton.