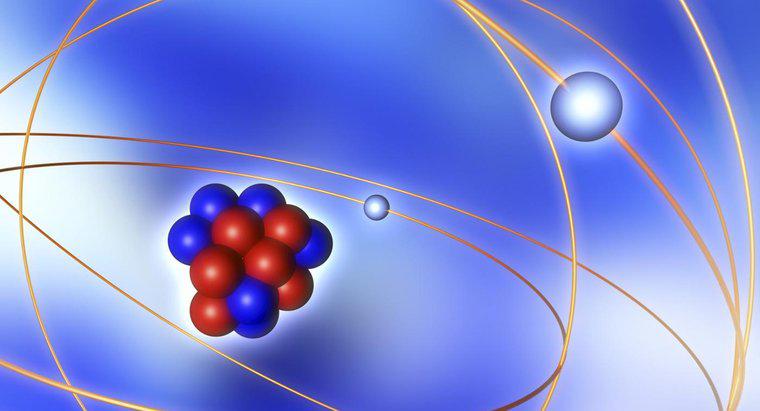
Hạt nhân của nguyên tử được bao quanh bởi một đám mây electron được giữ cố định bởi lực điện từ. Hạt nhân chiếm nhiều hơn đáng kể trong tổng khối lượng của nguyên tử so với đám mây, mặc dù đám mây chiếm để có thể tích nguyên tử lớn hơn.
Một nguyên tử có ba khối cấu tạo: proton, neutron và electron. Hạt nhân nằm ở trung tâm bao gồm các proton mang điện tích dương và các neutron trung hòa. Các vật phẩm này được liên kết với nhau bởi một lực hạt nhân. Số proton trong hạt nhân xác định nguyên tử thuộc về nguyên tố nào, thường được gọi là số hiệu nguyên tử. Đám mây electron xung quanh hoàn toàn bao gồm các electron mang điện tích âm. Mặc dù có hạt nhân và đám mây xung quanh, phần lớn nguyên tử là không gian trống.
Mô hình đám mây không phải là khái niệm đầu tiên. Một số mô hình đã được xem xét trước khi đám mây được chấp nhận vào những năm 1920. Các mô hình trước đó bao gồm các mô hình Billiard Ball và Plum Pudding. Mô hình Bohr đã được áp dụng trong thế kỷ XX. Trong mô hình này, nguyên tử tương tự như một hệ mặt trời.
Một electron có điện tích 1,0671 x 10 ^ -19 coulomb. Một tính chất quan trọng của electron là spin. Spin trên một electron là tốc độ cụ thể bằng 1/2 lần một đơn vị quay, có thể được ấn định bởi cá nhân thực hiện phép đo.