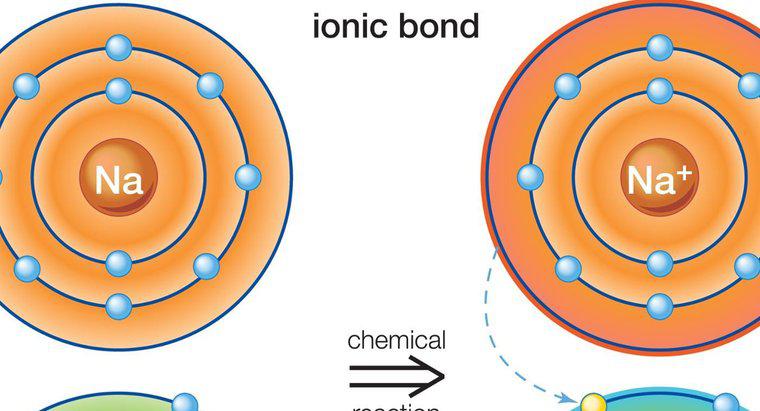
Hợp chất ion là chất rắn, có nhiệt độ nóng chảy cao, dẫn điện, cứng nhưng giòn và được hình thành từ liên kết ion giữa một kim loại và một phi kim. Liên kết ion là liên kết giữa hai nguyên tố với các điện tích trái dấu. Các điện tích trái dấu sẽ hút nhau, tạo ra một liên kết hóa học bền chặt.
Các hợp chất ion hòa tan dễ dàng trong các dung môi phân cực, chẳng hạn như nước. Chúng không hòa tan dễ dàng trong các dung môi không phân cực, bao gồm ête và xăng. Điều này là do các hợp chất ion có xu hướng hình thành các phân tử phân cực, chúng hòa tan trong các dung dịch có độ phân cực tương tự. Dung môi không phân cực không cung cấp đủ năng lượng để phá vỡ liên kết ion và làm tan cấu trúc tinh thể của hợp chất.
Các tính chất dẫn điện của các hợp chất ion áp dụng khi chúng được hòa tan trong dung dịch ion hoặc khi chúng bị nóng chảy. Khi các hợp chất ion ở thể rắn, chúng là chất cách điện hơn là chất dẫn điện. Điều này là do các điện tích không thể đi qua cấu trúc mạng tinh thể chặt chẽ của một hợp chất ion ở trạng thái rắn.Natri clorua, còn được gọi là muối ăn; kali clorua, được sử dụng trong y tế và như một chất thay thế muối; và corundum, khoáng chất mà hồng ngọc và ngọc bích được tạo thành, là các hợp chất ion nổi tiếng. Tất cả các hợp chất này tạo nên cấu trúc tinh thể, một đặc điểm chung khác của các hợp chất ion.