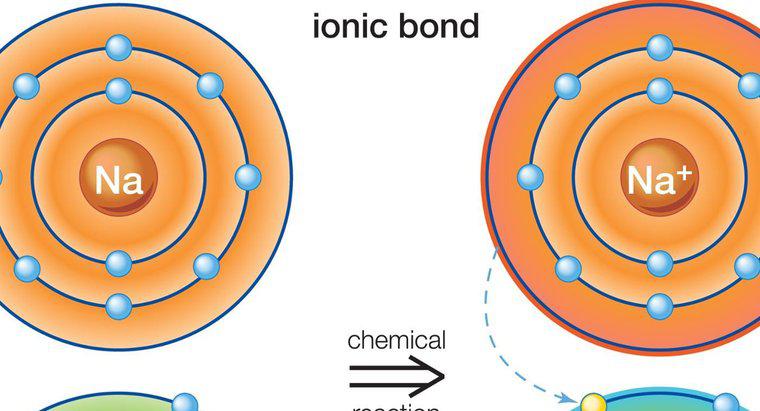
Các hợp chất ion trung hòa về điện vì điện tích của các cation và anion tạo nên hợp chất triệt tiêu lẫn nhau. Trong trường hợp muối, ví dụ, natri có điện tích dương, và clorua có điện tích âm. Cùng nhau, chúng trung hòa hợp chất.
Hợp chất ion được tạo thành từ các nguyên tử hoặc phân tử mang điện tích dương và âm. Những chất mang điện tích dương được gọi là cation, trong khi những chất mang điện tích âm được gọi là anion. Cả hai hút nhau vì điện tích trái dấu. Các cation và anion có thể thu hút nhiều hơn một phân tử khác loại, tạo ra một phân tử dài hơn được liên kết với nhau bằng liên kết ion.
Canxi clorua là một ví dụ khác về hợp chất ion, với canxi dương khử clorua âm. Sắt bromua cũng làm như vậy, với điện tích dương từ sắt triệt tiêu điện tích âm từ bromua. Tính trung hòa về điện này giúp giữ cho hợp chất ổn định, giúp hợp chất này hoạt động dễ dàng hơn và ít bay hơi hơn nhiều so với các ion không ổn định.
Hầu hết các hợp chất ion là chất rắn có nhiệt độ nóng chảy cao. Chúng thường được tạo thành bởi một kim loại và một nguyên tố phi kim loại. Các hợp chất được tạo ra từ hai phi kim thường là các hợp chất liên kết cộng hóa trị.