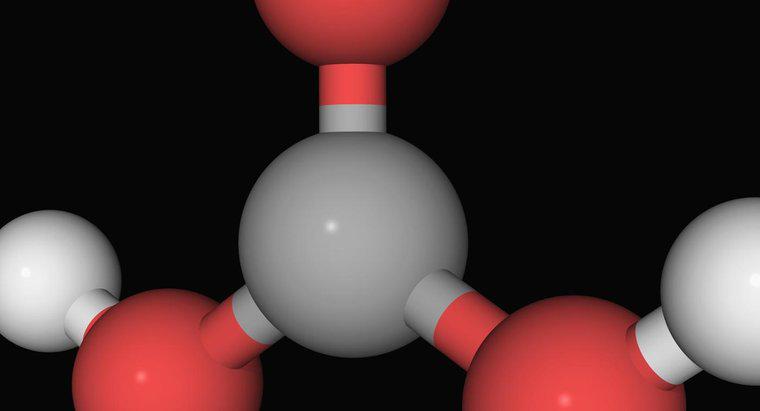
Phương trình cân bằng cho sự hình thành axit cacbonic là CO2 + H 2 OH 2 CO 2 H + + HCO 3- . Axit cacbonic hình thành từ sự hòa tan của nước, hoặc H 2 O, trong carbon dioxide, hoặc CO 2 .
Axit cacbonic, hoặc H 2 CO 3 , là một axit yếu đóng vai trò quan trọng trong việc hô hấp, duy trì phạm vi bình thường của pH trong máu, hiện tượng nóng lên toàn cầu , và cacbonat hóa đồ uống. Trong dung dịch lỏng, axit cacbonic dễ dàng liên kết thành ion bicacbonat tích điện (HCO 3- ) và proton (H +). Khi CO 2 hình thành trong quá trình trao đổi chất trong tế bào, nó sẽ chuyển đổi thành bicarbonate, một ion. Sự chuyển đổi này cho phép vận chuyển nó trong máu vào phổi, nơi bicarbonate chuyển hóa trở lại thành CO2 để thở ra.
Ở động vật có vú, quá trình tương tự cũng xảy ra bởi carbonic anhydrase, một loại enzyme có thể tăng tốc độ phản ứng qua lại giữa việc sản xuất axit cacbonic và chuyển hóa nó thành carbon dioxide và nước. Bicarbonate cũng được sử dụng trong các cơ sở y tế, bao gồm cả như một biện pháp tạm thời trong hồi sinh tim phổi để cố gắng chống lại tình trạng nhiễm toan hoặc đảo ngược quá liều trong thuốc chống trầm cảm ba vòng, do khả năng đệm pH của máu.
Nếu có quá nhiều axit (H +) trong dung dịch, cân bằng sẽ chuyển sang sự chuyển đổi bicacbonat (HCO 3- ) thành axit cacbonic (H 2 CO 3 ) sau đó có thể tạo thành CO 2 + H 2 O. Quá trình này làm giảm lượng axit trong máu. Trong khi thở quá mức, mọi người thở ra quá nhiều CO 2 , và phương trình chuyển sang sản xuất CO 2 và sử dụng axit trong máu, do đó gây ra nhiễm kiềm hô hấp. Việc không thở hết CO 2 , chẳng hạn như trong chứng ngưng thở khi ngủ do tắc nghẽn, sẽ làm thay đổi trạng thái cân bằng đối với việc sản xuất axit cacbonic và cuối cùng là axit hóa máu.