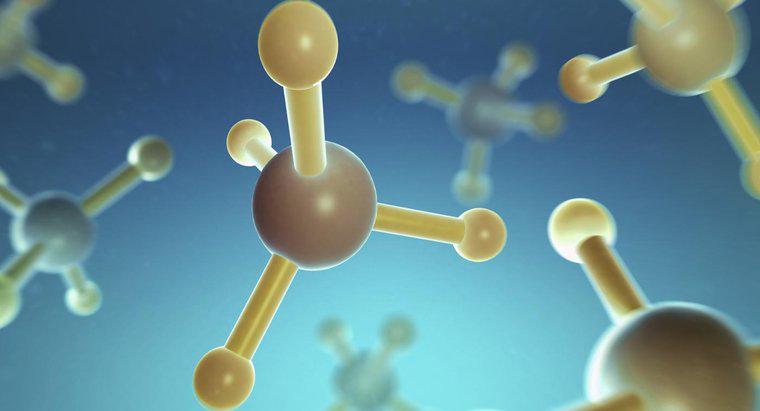
Lưu huỳnh tetrafluoride, viết tắt là SF4, có dạng hình học điện tử ba góc ba cạnh. Điều này có nghĩa là nguyên tử lưu huỳnh trung tâm được liên kết với bốn nguyên tử flo và có một cặp điện tử duy nhất.
Theo lý thuyết lực đẩy cặp electron lớp vỏ hóa trị, các nguyên tử và cặp đơn lẻ sẽ di chuyển càng xa nhau càng tốt, trong trường hợp này tạo ra một cấu hình lưỡng tháp tam giác. Cấu trúc này bao gồm một mặt phẳng phẳng của hai flo và một cặp đơn lẻ, giống như cấu trúc của một phân tử phẳng tam giác. Trên và dưới mặt phẳng (ở đầu và cuối phân tử) có thêm hai flo. Các cặp đơn lẻ chiếm nhiều không gian hơn các nguyên tử; do đó, một cặp duy nhất nằm trong mặt phẳng vì điều đó cho phép nó ở xa nhất so với các phân tử khác.