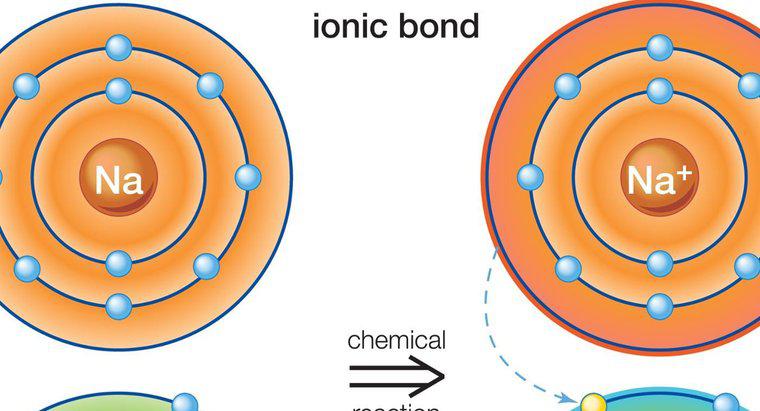
Các nguyên tử lớn hơn có obitan electron phức tạp, chẳng hạn như các obitan được tìm thấy trong các kim loại chuyển tiếp, có thể vượt quá quy tắc octet trong các điều kiện thích hợp. Đặc biệt, những nguyên tử này xảy ra khi các nguyên tố nặng hơn được liên kết với các nguyên tố nhỏ, có độ âm điện cao như flo, clo hoặc oxy. Một ví dụ là photpho pentachlorua, một nguyên tử photpho đơn liên kết với năm nguyên tử clo, có 10 điện tử dùng chung trong lớp vỏ hóa trị ngoài cùng của nó.
Khi một nguyên tố có số hiệu nguyên tử đủ cao, một loại quỹ đạo electron mới sẽ có sẵn với khả năng chứa tối đa 10 electron, cho phép tối đa 5 liên kết đơn. Đây là những gì xảy ra với photpho pentachlorua. Tuy nhiên, để sử dụng quỹ đạo đó, phản ứng tạo ra hợp chất sử dụng quỹ đạo này phải rất thuận lợi về mặt năng lượng. Đây là lý do tại sao, để làm cho nó hoạt động, các nguyên tố có khả năng hút và liên kết electron rất mạnh, còn được gọi là độ âm điện, phải tham gia. Oxy có độ âm điện lớn, nhưng nó khó có thể tạo ra một hợp chất có năm nguyên tử liên kết như clo, vì nó cần hai electron để hoàn thành lớp vỏ hóa trị ngoài cùng của nó. Flo và clo mỗi loại chỉ yêu cầu một và do đó, loại cấu hình này có nhiều khả năng xảy ra hơn.