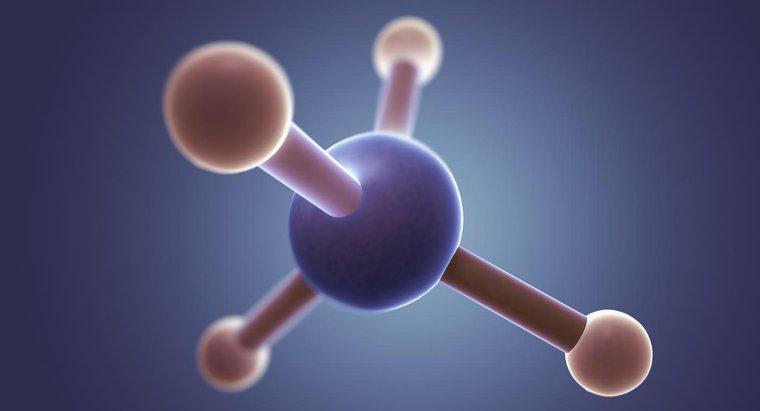
CF4, hoặc tetrafluoromethane, là một phân tử tứ diện. Như được chỉ ra bởi phần "tứ diện" của tên, phân tử có bốn nhóm electron liên kết xung quanh một nguyên tử trung tâm.
Cũng như nhiều liên kết electron, phân tử tứ diện có một số phần. Phần chính của phân tử là nguyên tử, luôn nằm ở trung tâm. Bốn nhóm electron được đặt cách nhau xung quanh nguyên tử. Các electron này không bao giờ nằm trong các cặp đơn lẻ và chúng luôn ở cùng nhau theo một mô hình đồng đều xung quanh nguyên tử, mặc dù chúng không phải lúc nào cũng có khoảng cách bằng nhau.
Bởi vì các điện tử bị flo thu hút nhiều hơn so với cacbon, các điện tử dành nhiều thời gian hơn để gần flo hơn trong mô hình CF4. Các điện tử được giữ lại với nhau bằng các liên kết cộng hóa trị, và các liên kết này kéo về phía flo và kéo ra khỏi cacbon. Mặc dù flo và cacbon có phần bằng nhau nhưng flo có lực kéo mạnh hơn. Công thức hóa học CF4 phản ánh lực kéo của các electron đối với flo lớn hơn. Việc thiếu một số với carbon cho thấy các electron không bị kéo về phía carbon mà bị đẩy ra khỏi nó.