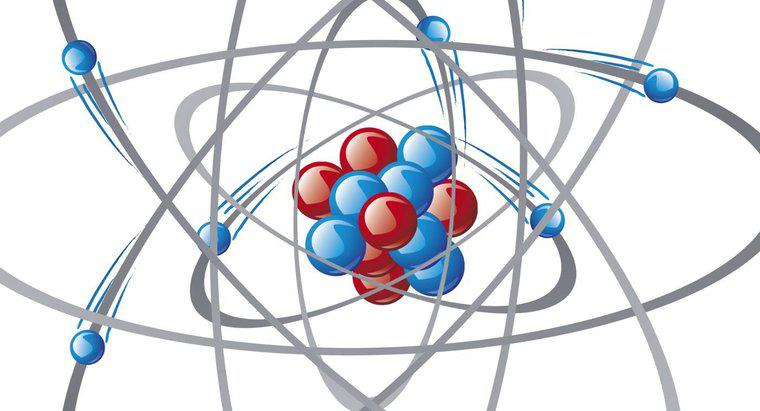
Hình học phân tử của dichlorine monoxide bị bẻ cong do các cặp electron đơn lẻ nằm trên nguyên tử oxy. Hình học phân tử là biểu diễn vật lý về mối quan hệ giữa các nguyên tố trong một hợp chất.
Hình học phân tử được đặc trưng bởi Mô hình Lực đẩy cặp điện tử Valence Shell. Mô hình ba chiều này dựa trên lực đẩy giữa các cặp electron. Nó bắt đầu với nguyên tắc rằng quy tắc octet phải được thỏa mãn cho mỗi phần tử. Điều này có nghĩa là mỗi nguyên tố phải có tám electron hóa trị ở lớp vỏ ngoài cùng. Vì nhiều nguyên tố không có tám điện tử hóa trị trong lớp vỏ ngoài cùng của chúng, kết quả là sự chia sẻ điện tử. Các electron không được chia sẻ được minh họa bằng các dấu chấm.
Có tổng cộng 13 dạng hình học phân tử. Các dạng hình học này được phân biệt với nhau bởi một số yếu tố, bao gồm số lượng nhóm liên kết và cặp electron đơn lẻ trên nguyên tử trung tâm. Một yếu tố bổ sung là hình học của cặp electron, có thể là một trong năm kiểu. Điều này rất quan trọng đối với dichlorine monoxide vì có hai dạng hình học phân tử được phân loại là uốn cong. Bởi vì nguyên tử oxy trung tâm có hai cặp electron đơn lẻ, nó được xếp vào dạng uốn cong tứ diện hơn là bẻ cong tam giác. Sự hình thành hình học này được đặc trưng bởi các góc liên kết nhỏ hơn 109,5 độ.